Farmacocinética es la ciencia que cuantifica cómo se absorben, distribuyen, metabolizan y excretan los fármacos en el organismo. Para describir con precisión estos procesos, los científicos utilizan modelos matemáticos, principalmentemodelos de compartimentosymodelos no compartimentadosComprender estos modelos es esencial para interpretar los datos farmacocinéticos y optimizar el desarrollo de fármacos y las estrategias de dosificación. En este artículo, exploraremos los conceptos básicos de los modelos compartimentales y no compartimentales, sus aplicaciones y sus respectivas ventajas y desventajas.
Modelos de compartimentos
Definición y conceptoLos modelos compartimentados simplifican el cuerpo en espacios hipotéticos llamados compartimentos. Estos compartimentos no son entidades anatómicas o fisiológicas, sino más bien construcciones matemáticas que representan grupos de tejidos u órganos donde se supone que las tasas de distribución y eliminación de fármacos son uniformes.
Tipos de modelos de compartimentos
1. Modelo de un solo compartimento:
Descripción:En el modelo monocompartimental, el organismo se considera como un único compartimento homogéneo. Tras la administración, el fármaco se distribuye de forma instantánea y uniforme por todo el compartimento. La concentración del fármaco disminuye con el tiempo debido a los procesos de eliminación.
Solicitud:Este modelo se utiliza a menudo para medicamentos que se distribuyen rápidamente y de manera uniforme por todo el cuerpo, como los que se administran por vía intravenosa.
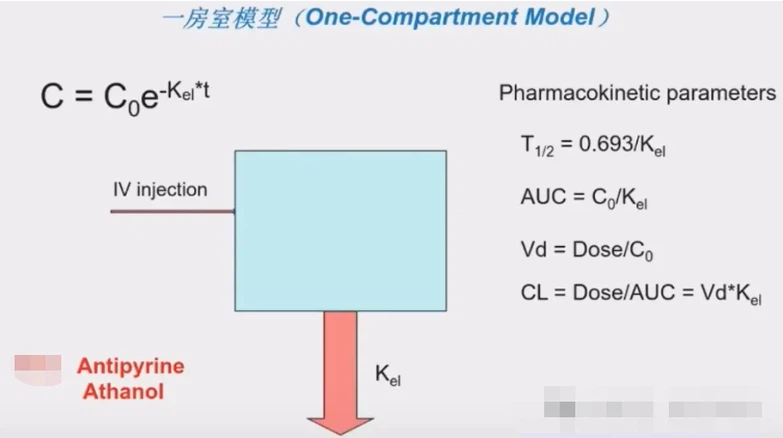
Parámetros clave:
- Kel(Constante de tasa de eliminación): La velocidad a la que el fármaco se elimina del organismo.
- t1/2(Vida media): Tiempo necesario para que la concentración del fármaco se reduzca a la mitad.
- Enfermedad venérea(Volumen de distribución): Volumen aparente en el que se distribuye el fármaco.
- CL(Aclaramiento): La velocidad a la que el fármaco se elimina del organismo.
2. Modelo de dos compartimentos:
Descripción:El cuerpo se divide en dos compartimentos: el compartimento central (órganos altamente perfundidos como el corazón, el hígado y los riñones) y el compartimento periférico (tejidos menos perfundidos como la grasa y los músculos). Después de la administración, el fármaco se distribuye rápidamente en el compartimento central y luego se equilibra lentamente con el compartimento periférico.
Solicitud:Adecuado para medicamentos que tienen una fase de distribución más lenta, donde la concentración del medicamento disminuye rápidamente al principio (fase de distribución) y luego más lentamente (fase de eliminación).
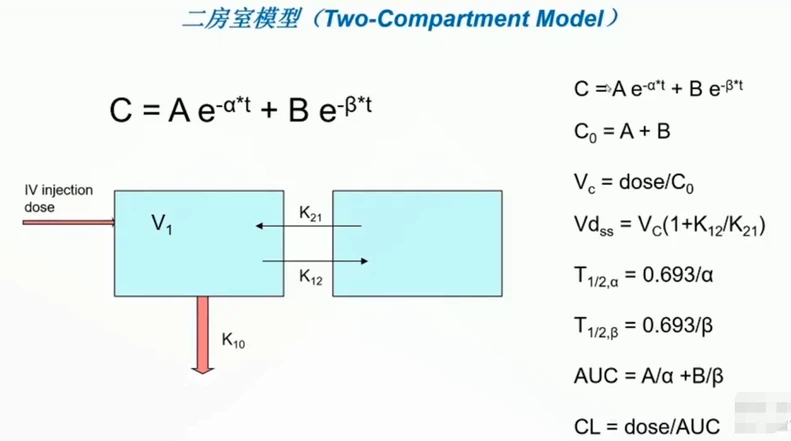
Parámetros clave:
- (Constante de tasa de distribución): La tasa de transferencia de fármaco entre los compartimentos central y periférico.
- (Constante de tasa de eliminación): La velocidad a la que se elimina el fármaco del compartimento central.
- V1(Volumen del Compartimento Central) yV2(Volumen del Compartimento Periférico): Representa los volúmenes aparentes en cada compartimento.
Ventajas de los modelos compartimentados:
- Sencillez:Fácil de entender y aplicar a datos farmacocinéticos básicos.
- Flexibilidad:Los investigadores pueden elegir el modelo apropiado en función del comportamiento del fármaco y los objetivos de la investigación.
- Poder descriptivo:Estos modelos pueden describir diferentes fases de la disposición de medicamentos, como la distribución y la eliminación.
Desventajas de los modelos compartimentados:
- Simplificación excesiva:No tienen en cuenta la naturaleza compleja y heterogénea de la distribución y eliminación de fármacos en el organismo.
- Inconsistencias:Distintos estudios o laboratorios podrían utilizar modelos diferentes, lo que dificulta las comparaciones.
Modelos sin compartimentos
Definición y conceptoModelos sin compartimentos, también conocidos comoteoría del momento estadísticoométodos independientes del modelo, no asumen ningún compartimento específico, sino que analizan el comportamiento general del fármaco en el organismo mediante métodos estadísticos.

Características de los modelos sin compartimentos:
- Perspectiva global:Este enfoque considera el comportamiento del fármaco como un todo, sin dividir el cuerpo en compartimentos.
- Simplicidad matemática:Utiliza herramientas estadísticas simples para calcular parámetros farmacocinéticos clave directamente a partir de los datos de concentración-tiempo del fármaco.
Parámetros:
- metro(Tiempo medio de residencia): El tiempo promedio que una molécula de fármaco permanece en el cuerpo.
- AUC(Área bajo la curva): La exposición total del cuerpo al fármaco a lo largo del tiempo.
- CL(Aclaramiento): Similar a los modelos compartimentados, representa la tasa de eliminación del fármaco.
Ventajas de los modelos sin compartimentos:
- Exactitud:Proporciona una representación más precisa del comportamiento del fármaco, especialmente para fármacos con patrones complejos de distribución y eliminación.
- Facilidad de comparación:Dado que no depende de supuestos sobre compartimentos específicos, permite una comparación más sencilla entre diferentes estudios y medicamentos.
- Flexibilidad:Se puede aplicar a cualquier fármaco que siga una farmacocinética lineal.
Desventajas de los modelos no compartimentados:
- Visión limitada:No proporciona información detallada sobre las diferentes fases de distribución y eliminación del fármaco.
- Sensibilidad:Los parámetros calculados pueden ser sensibles a las fluctuaciones en la fase terminal de la curva de concentración del fármaco-tiempo.
Tanto los modelos compartimentales como los no compartimentales son herramientas valiosas en farmacocinética. Los modelos compartimentales son más intuitivos y útiles para describir fases específicas del movimiento de un fármaco en el organismo, mientras que los modelos no compartimentales proporcionan una visión general más amplia y precisa de la cinética de los fármacos. Comprender estos modelos es fundamental para que los investigadores y los médicos puedan tomar decisiones informadas sobre la dosificación, la eficacia y la seguridad de los fármacos.
Para Prisys Biotech, especializada en investigación preclínica, estosmodelos Ofrecer los medios para interpretar datos farmacocinéticos complejos, mejorando así el desarrollo de nuevas terapias y garantizando su uso seguro y eficaz en entornos clínicos.